

 |
 |
|
Представлена версия документа, предназначенная для печати
Вы можете загрузить эту страницу на сайте
Anadara kagoshimensis (Tokunaga, 1906) |
Систематическое положение (Kingdom, Phylum, Class, Order, Family, Species):
Царство — Животные, Animalia, Тип — Моллюски, Mollusca, Класс — Двустворки, Bivalvia, Подкласс — Птериоморфы, Pteriomorphia, Отряд — Арциды, Arcida, Семейство — Арки, Arcidae, Род — Анадара, Anadara, Вид — Анадара кагошименсис, Anadara kagoshimensis

Русское и английское названия. Анадара Anadara
Синонимы. С момента первого обнаружения в Чёрном море в 1968 г. (Киселева, 1992) вид описывали под различными именами: Anadara sp. (Маринов и др., 1983; Нгуен Суан Ли, 1984), Cunearca cornea (Reeve, 1844) (Кънева-Абаджиева, Маринов, 1984; Золотарев, Золотарев, 1987; Маринов, 1990; Иванов, 1991; Киселева, 1992), Scapharca inaequivalvis (Bruguière, 1789) (Gomoiu, 1984), Anadara inaequivalvis (Bruguière, 1789) (Ревков и др., 2002, 2004; Occhipinti-Ambrogi, Savini, 2003; Anistratenko et al., 2014 и др.). Последнее название широко использовалось вплоть до 2010 г., когда вид был отнесен к Anadara kagoshimensis (Tokunaga, 1906) (Huber, 2010) с последующим подтверждением диагностики на генетическом уровне (Krapal et al., 2014). Примечательно, что одновременно с генетическим подтверждением видовой принадлежности черноморской анадары к A. kagoshimensis появилась работа (Anistratenko et al., 2014), указывающая на то, что границы и характер конхологической изменчивости Азово-Черноморской анадары соответствуют таковой A. inaequivalvis из типовой местности – Коромандельского побережья Индии.
Другие синонимы: Anadara sativa (Bernard, Cai & Morton, 1993); Arca (Scapharca) peitaihoensis Grabau & S. G. King, 1928; Scapharca sativa Bernard, Cai & Morton, 1993; Scapharca subcrenata (Lischke, 1869) (WoRMS Editorial Board, 2018).
Нативный ареал. A. kagoshimensis относится к тепловодным формам моллюсков (Лутаенко, 1999); широко распространена в Индо-Пацифике: от Индии и Шри-Ланка до Индонезии, и от Японии до северного побережья Австралии (Poutiers, 1998).
Современный ареал (мировой и конкретнее в России). Включает район Индо-Пацифики, бассейн Средиземного, с центром инвазии в Адриатическом море (Ghisotti, 1973), Чёрное и Азовское моря. Схема освоения Азово-Черноморского бассейна (см. карту) и особенности формирования сообществ анадары представлены в работе Н.К. Ревкова (2016). Отмечена этапность инвазионного процесса. После первого обнаружения у берегов Кавказа в 1968 г. (Киселева, 1992) ее массовые поселения появились у западных и восточных берегов Чёрного моря только в 1980-х гг. (Маринов и др., 1983; Gomoiu, 1984; Золотарев В., Золотарев П., 1987; Маринов, 1990; Киселева, 1992; Иванов, Синегуб, 2008 и др.), а у берегов Турции – в 1990-х гг. (Sahin et al., 2009). Первые находки анадары у берегов Крыма датируются концом 1990-х – началом 2000-х гг. (Ревков и др., 2002, 2004). Однако довольно быстро из малозаметного вселенца уже к 2013 г. на ряде участков Крымского шельфа она превратилась в одну из руководящих форм бентоса (Ревков, 2015). Запаздывание (приблизительно 20–25 лет) появления анадары на крымском и анатолийском участках черноморского шельфа при наличии уже сложившихся ее поселений на западном и восточном побережье Чёрного моря объясняется существованием гидрологических барьеров, препятствующих свободному вдольбереговому переносу планктонных личинок (Ревков, 2016).
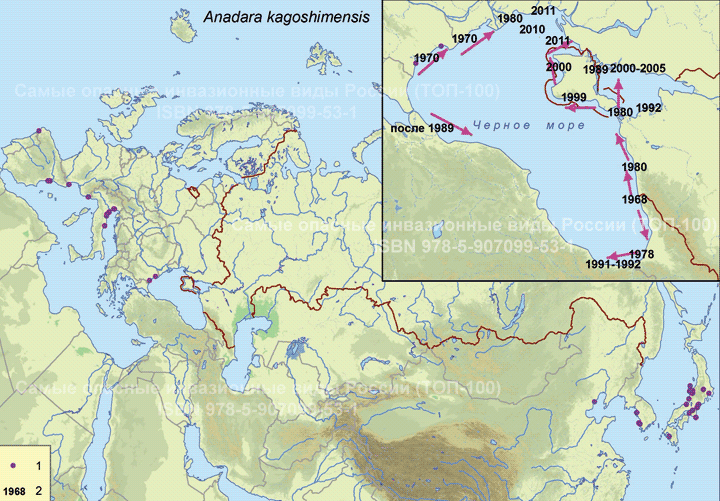
Пути(коридоры) и векторы (способы) интродукции. Появление анадары в Чёрном море связывают с судоходством, вызвавшим случайный занос личинок с балластными водами (Zaitsev, Mamaev, 1997; Шиганова, 2009) из умеренных широт северной части Тихого океана (Zenetos et al., 2010).
Местообитание. A. kagoshimensis относится к тепловодным формам моллюсков (Лутаенко, 1999), однако устойчивое развитие её поселений в «жёстких» температурных условиях Чёрного и Азовского морей свидетельствует о биологической эвритермности вида – способности существовать в широких границах изменения температуры. Анадара является эвригалинным видом (Broom, 1980), легко переносит гипоксические и аноксические условия (Isani et al., 1986). Несмотря на то, что максимальное ее распространение соответствует областям с соленостью около 30 ‰, моллюск переносит опреснение до 10–11‰ (Чихачев и др., 1994), а в Андриатике встречается даже в солоноватоводных лагунах (Rinaldi, 1985).
Анадара в основном является обитателем мягких субстратов (песчаных и илистых) (Zaitsev, Mamaev, 1997) в диапазоне глубин от 3–60 м (Маринов, 1990; Sahin et al., 2009; Ревков, 2015). В Азовском море встречается на глубинах до 10–11 м (Чихачев и др., 1994). Максимальное развитие данный вид получил в обогащённых органикой приустьевых участках западного и восточного черноморского шельфа (Чикина, 2009; Abaza et al., 2010; Gomoiu, 2005).
Некоторые особенности биологии. Анадара – раздельнополое животное. Клетки содержат 38 хромосом (2n) (Corni et al., 1988). Половое созревание происходит на 2–3-м году жизни при длине раковины около 10–20 мм (Чикина и др., 2003; Sahin et al., 2006). Массовый нерест моллюсков наблюдается летом – с июня по сентябрь при достижении температуры воды более 20°С (Чикина и др., 2003; Sahin et al., 2006), с возможной пролонгацией до октября. С ноября по февраль в развитии гонад самцов и самок наблюдается фаза покоя (Sahin et al., 2006). Планктонные личинки предпочитают верхние водные горизонты (0–25 м) (Казанкова, 2002). Продолжительность развития личинки до стадии трохофоры – 6 часов, велигера – 23 часа (Пиркова, 2012). Поздние личинки имеют удлиненно-овальную интенсивно окрашенную красно-коричневую раковину и пигментный глазок (Казанкова, 2002). В условиях Чёрного моря в сравнении с другими акваториями Мирового океана темп роста A. kagoshimensis несколько выше (Sahin et al., 2006), что объясняется более благоприятными кормовыми условиями. Максимальный возраст A. kagoshimensis (7 лет) зарегистрирован в популяции моллюсков восточной части анатолийского побережья (Sahin et al., 2009), здесь же отмечена и наибольшая длина черноморских экземпляров – до 85 мм. На кавказском побережье и у берегов Болгарии длина раковины анадары не превышает 60 мм (Золотарев, Терентьев, 2012; Маринов, 1990), в Керченском проливе – 65 мм (Анистратенко, Халиман, 2006). В Азовском море максимальный возраст моллюсков оценивается в 5–6 лет при средней длине ~50 мм (Чихачев и др., 1994). По типу питания анадара относится к фильтраторам-сестонофагам.
Анадара имеет высокоэффективный анаэробный тканевой метаболизм. Это позволяет ей длительный период времени пережидать условия экстремальной гипоксии и аноксии (Солдатов и др., 2008). Адаптивная способность анадары к таким условиям во многом зависит от свойств гемолимфы, содержащей многочисленные эритроциты, и три вида белых клеток (Holden et al., 1994; Novitskaya, Soldatov, 2013). Эритроцитарный гемоглобин обеспечивает высокую кислородную емкость гемолимфы. Даже при чрезвычайных низких концентрациях кислорода (менее 1.2% насыщения) моллюск удерживает норму его потребления (Cortesi et al., 1992), а в условиях аноксии показывает самое высокое сохранение энергии (Soldatov et al., 2009). Последнее связано с переходом на аспартат-сукцинатное направление метаболизма, которое может обеспечить достаточный ресинтез ATФ в условиях анаэробиоза (Soldatov et al., 2010).
Влияние вида (на другие виды, экосистемы включая лесную и агроценозы, здоровье человека). В бассейне Средиземного моря A. kagoshimensis отнесена к локально инвазивной группе видов (Gofas, Zenetos, 2003; Zenetos et al., 2010). В Азово-Черноморском регионе массовое развитие вида-вселенца определило пространственно более широкий (в целом «бассейновый») масштаб его влияния на аборигенные виды и экосистему в целом. За недолгий промежуток времени из малозаметного вселенца анадара превратилась в ценозообразующий вид, стала субъектом и причиной трансформации донных экосистем практически на всём протяжении черноморского шельфа в диапазоне глубин до 49 м и в акватории Азовского моря.
Биотические взаимоотношения анадары с аборигенными видами Азово-Черноморского бассейна еще мало изучены. В фаунистическом плане у открытых берегов Крыма анадару следует отнести к донному комплексу видов мидийного пояса бентали (Ревков и др., 2015), в котором она тяготеет к другому доминанту – двустворчатому моллюску Pitar rudis, входя в состав формируемого им сообщества (Ревков, 2015), или образует с ним смешанный биоценоз (Феодосийский залив, глубина 28–34 м) (Болтачева и др., 2011). На кавказском побережье на глубине 20–30 м формирует собственный биоценоз (Чикина, 2009). В Варненской бухте на заиленных песках на глубине 7 м выступает кодоминантом в сообществе Upogebia pusilla + Tellina tenuis (Trayanova et al., 2011). На Филлофорном поле Зернова (северо-западный шельф Чёрного моря) на глубинах 14–49 м она встречена в составе биоценотического комплекса Mytilus galloprovincialis (Ревков, 2015). В любом из перечисленных выше биотических комплексов, при дефиците пищи анадара может вступать в конкурентные отношения с аборигенными видами из группы фильтраиторов-сестонофагов, включая промысловую черноморскую мидию. В связи с этим отметим, что существующие в настоящее время данные по вытеснению анадарой аборигенных видов двустворчатых моллюсков из некоторых совместных зон обитания – пока носят предположительный характер (Анистратенко, Халиман, 2006; Милютин, Вилкова, 2006). Учитывая широкие адаптационные возможности анадары к условиям среды, её устойчивость к заилению и дефициту кислорода, нельзя исключать наличие не вытеснения, а «компенсаторного» замещении анадарой аборигенных видов в условиях изменения качества биотопа (Ревков, Щербань, 2017).
Массовое развитие поселений анадары происходило на пике эвтрофирования бассейна Чёрного моря (1980–1990-е гг.). По-видимому, здесь можно говорить о положительной роли вида-вселенца: феномене появления и массового развития в Чёрном море анадары в период её наибольшей востребованности как потребителя избыточного органического вещества (Ревков и др., 2015).
Анадара – съедобный моллюск, что позволяет рекомендовать её в качестве объекта промысла и марикультуры. Специальные исследования показали, что ткани анадары содержат ценные в пищевом отношении каротиноиды: β-каротин, пектенол А, пектенолон (транс- и цис-изомеры), зеаксантин, диа-токсантин, аллоксантин, а также эфиры алло- и диатоксантинов (Бородина, Солдатов, 2016).
Контроль численности. Наиболее уязвимыми в жизненном цикле анадары, наряду с личиночным развитием, являются первые два года жизни. В этот период моллюски, в силу недостаточной прочности створок раковины, являются доступным кормовым объектом для брюхоного моллюска-рапаны и рыб-бентофагов (Чихачев и др., 1994). Трофический статус акватории в районах развития поселений анадары и пищевой пресс – являются одними из ведущих факторов, стабилизирующих численность моллюсков. Анализ материалов по биомассе и численности позволил прийти к заключению о фактической реализации анадарой в условиях Чёрного моря своего биотического потенциала на западном и восточном участках шельфа (Ревков, 2016).
Авторы.Солдатов А.А., Ревков Н.К., Петросян В.Г.
|
Графическое представление перекрывания ниш нативной и инвазионной частей ареалов, а также при сценариях изменения климата |
|
|
Текущий климат |
|
|
Нативная часть |
Инвазионная часть |
|
|
|
| Графическое представление перекрывания ниш нативной (A) и инвазионной (B) частей ареалов вида, где сиреневый цвет – зона стабильности, розовый цвет – зона расширения, зеленый цвет – зона «неиспользования». Сплошные и пунктирные линии показывают 100% и 90% области доступной среды в нативной (черные линии) и инвазионной (красные линии) частях ареалов, которые использовались для анализа перекрывания ниш. | |
|
Сценарии изменения климата |
|
|
RCP26 |
RCP45 |
|
|
|
|
RCP60 |
RCP85 |
|
|
|
| Графическое представление перекрывания ниш в условиях текущего климата и при сценариях его изменения - (C) RCP26; (D) RCP45; (E) RCP60; (F) RCP85. | |
Литература.
| |
| Web-портал Инвазионные виды на территории России разработан и поддерживается кабинетом «Биоинформатики и моделирования биологических процессов» ИПЭЭ РАН в рамках выполнения гранта РНФ № 16-14-10323. | |
| © 2004-. Кабинет "Биоинформатики и моделирования биологических процессов" ИПЭЭ РАН | |